綜合新聞
博士研究生陳越等在《Emerging Microbes& Infections》雜志在線發表基于HIV單鏈抗體和雙功能抑制劑的基因治療策略的研究結果
艾滋病毒(HIV)的流行是人類健康的主要威脅之一,目前對于HIV的治療以多種抗病毒藥物聯合使用的“雞尾酒療法”為主。但耐藥株的出現和長期服藥的毒副作用使該療法也面臨著巨大挑戰。在過去的二十多年里,探索HIV功能性治愈甚至根除治愈的策略研究取得了一定進展。其中通過基因治療的方式,構建具有HIV抗性的造血干細胞(HSCs)或T淋巴細胞,模仿“柏林病人”和“倫敦病人”的成功案例,有潛力達到治愈或功能性治愈艾滋病的目的。
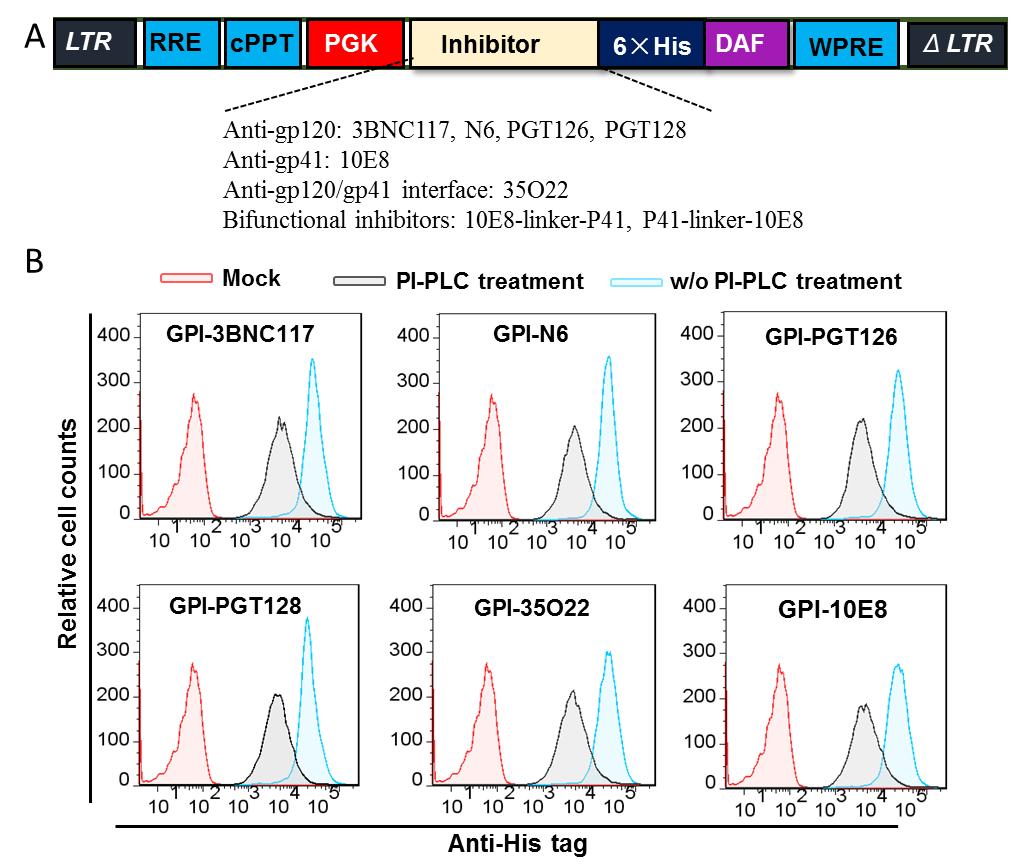
何玉先課題組在前期研究中已先后成功通過GPI脂錨方式分別將多肽膜融合抑制劑,靶向gp120的HIV納米抗體錨定于靶細胞膜上,獲得了HIV抗性細胞。本研究選取了一組近年來報道的具有強效抗病毒作用的廣譜中和抗體,將這些中和抗體的單鏈可變區分別通過GPI錨定于細胞膜上。經驗證,通過GPI脂錨平臺,靶向不同位點的中和抗體單鏈可變區展現出不同程度的對游離病毒(Cell-free virus)和細胞相關病毒(Cell-associated virus)的入侵和感染的抑制作用。其中GPI-10E8修飾的細胞具有最強效且廣譜的HIV抑制作用。通過機制上的研究發現GPI-10E8能夠干擾病毒包膜蛋白(Env)的加工,降低了子代病毒的感染性。進一步研究將中和抗體10E8的單鏈可變區與多肽膜融合抑制劑聯合,設計了靶向gp41的雙功能抑制劑。通過GPI脂錨方式,表達雙功能抑制劑的修飾細胞對HIV-1、HIV-2以及SIV均展現出相當強的抗性。本研究提供了制備HIV抗性細胞的新策略,在更深入的基因治療研究中,該策略可以單獨或與其他基因療法一起使用。
研究結果以“Cell membrane-anchored anti-HIV single-chain antibodies and bifunctional inhibitors targeting the gp41 fusion protein: new strategies for HIV gene therapy”為題在線發表于《Emerging Microbes & Infections》雜志。該項研究得到了中國醫學科學院醫學與健康科技創新工程、國家科技重大專項與國家自然科學基金等項目的支持。