綜合新聞
博士研究生于丹葳等在《Journal of Virology》在線發表關于新型HIV融合抑制劑在恒河猴模型治療效果及體內耐藥機制的研究論文
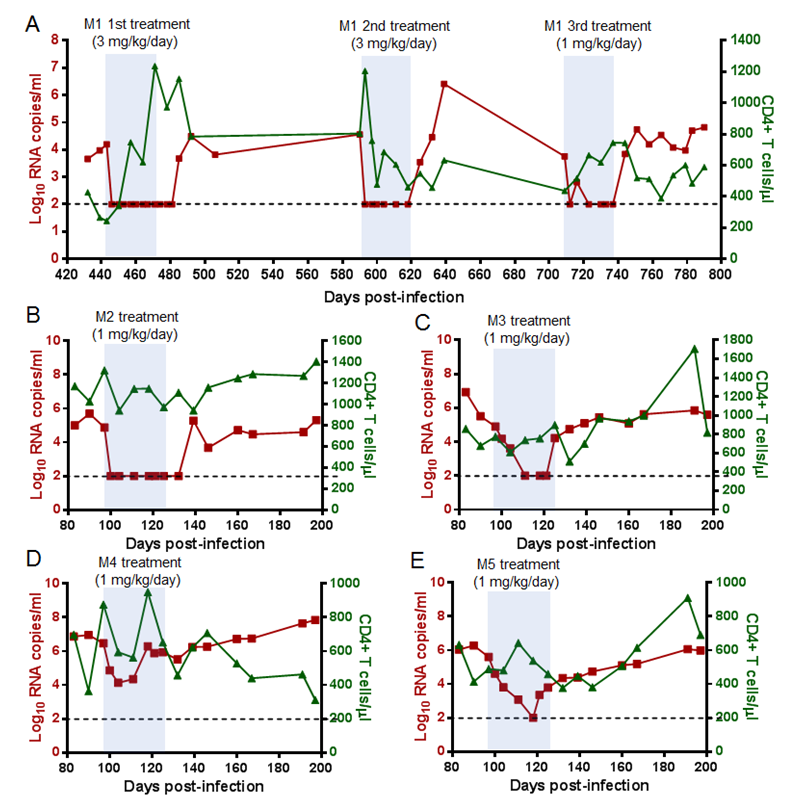
多肽藥物恩夫韋肽 (T20)是目前美國FDA批準上市的唯一病毒膜融合抑制劑,用于HIV感染的聯合治療,但由于其抗病毒活性較低,半衰期較短,且容易誘導耐藥,研發新型靶向HIV膜融合過程的藥物一直是國內外熱點課題。何玉先課題組多年來致力于HIV融合蛋白的結構與功能研究以及膜融合抑制劑的開發,其中“利普韋肽”(LP-80)已完成藥學、安全毒理和體內外藥效等臨床前研究內容,并于近期提交臨床試驗申請。本論文利用猴艾滋病病毒SIV感染的恒河猴模型對先導化合物LP-52在體內的治療效果及耐藥機制進行了探討,結果表明低劑量LP-52單藥治療可以迅速將恒河猴血漿病毒載量降低至檢測限以下水平。進一步利用出現病毒反彈的猴子標本,深入研究了LP-52在體內誘導耐藥的分子機制,發現 SIV包膜蛋白V562A,V562M和E657G的突變可以介導對LP-52的高度耐藥,并且對T20和LP-80等存在交叉耐藥現象。該研究的科學意義總結為三個方面:(1)驗證了了LP-52對SIV亦有強效的抗病毒效果;(2)發現基于脂肽的新型抑制劑與T20具有相同的耐藥途徑;(3)首次揭示SIV和HIV-1對病毒膜融合抑制劑具有類似的耐藥機制。